Gli Aminoacidi delle Proteine - riassunto e tabella - biologia - 2023
Che cosa sono gli aminoacidi?
Gli aminoacidi sono molecole organiche che contengono il gruppo acido peculiare dei composti organici (COOH) e il gruppo basico (NH2) o gruppo amminico legati al carbonio.
Quando lo stesso atomo di carbonio lega entrambi i gruppi si definiscono α (alfa) amminoacidi e venti di loro sono i mattoni fondamentali delle proteine.
Ogni molecola di aminoacido delle proteine è composta da quattro componenti chiave:
Tre di essi sono comuni a tutti e venti gli aminoacidi:
- un gruppo [basico] amminico (NH2),
- un gruppo [acido] carbossilico (COOH),
- un atomo di idrogeno (H).
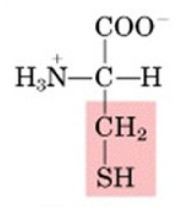
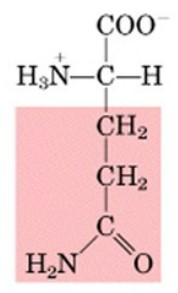
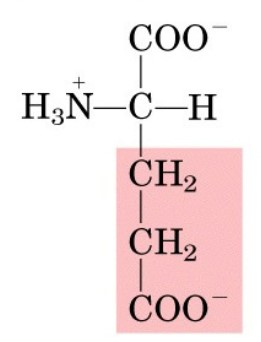
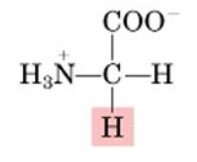
Il quarto gruppo o catena laterale R è invece variabile e diverso per ogni aminoacido.
Questi componenti si uniscono intorno a un carbonio centrale chiamato carbonio α (alfa) impegnato quindi in 4 legami con 4 gruppi diversi
Questa configurazione lo rende chirale: cioè in grado di assumere due configurazioni speculari e non sovrapponibili nello spazio: L e D.
Ebbene, i venti aminoacidi che servono per costruire le Proteine hanno tutti configurazione L
Perché i 20 aminoacidi delle proteine sono tutti L-aminoacidi?
La predominanza degli aminoacidi L all'interno delle proteine biologiche è principalmente dovuta ala fatto che le proteine vengono sintetizzate attraverso un processo molto complesso chiamato traduzione, che coinvolge l'assemblaggio di catene di aminoacidi (polipeptidi) sotto la guida dell'RNA messaggero (mRNA).
Tutte le tappe della traduzione sono catalizzate da enzimi specifici all'interno dei ribosomi, che sono in grado di riconoscere e selezionare soltanto una delle due forme speculari, L o D, dell'aminoacido. Gli enzimi coinvolti nella sintesi proteica hanno una specificità per gli aminoacidi in forma L. Questo processo selettivo favorisce l'incorporazione di esclusivamente aminoacidi L nella catena polipeptidica durante la sintesi proteica all'interno delle cellule.
Le fabbriche molecolari che prediligono la forma L sono quelle che sono state selezionate dall'evoluzione e sono state selezionate dalle prime cellule diffondendosi in tutte le forme viventi.
Quindi sebbene nelle cellule possono esistere D-aminoacidi e svolgere diversi ruoli come metaboliti i D-aminoacidi NON sono incorporati nelle proteine.
Quali sono i 20 aminoacidi presenti nelle proteine e codificati nel codice genetico?
Perché i gruppi degli aminoacidi sono carichi nelle immagini della tabella?
Nota Bene: Dato che il gruppo COOH è acido, in soluzione acquosa, come nell'ambiente interno delle cellule, dona un elettrone all'acqua e si trasforma in -COO-
Dato che il gruppo NH2 è basico, in soluzione acquosa, come nell'ambiente interno delle cellule, prende un elettrone dall'acqua e si trasforma in -NH3+
Le classi di Aminoacidi
Possiamo raggruppare gli aminoacidi a seconda della natura del gruppo R in 4 categorie principali:
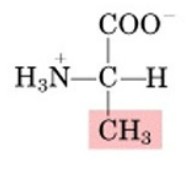
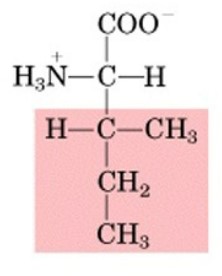
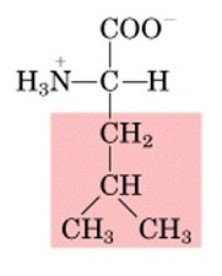
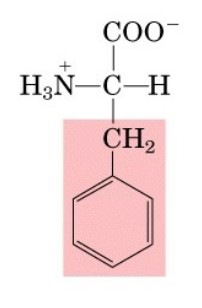
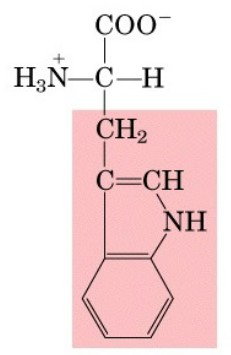
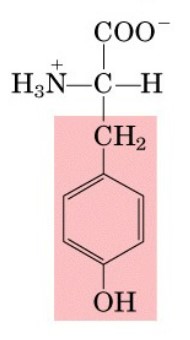
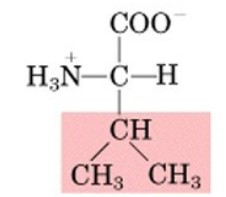
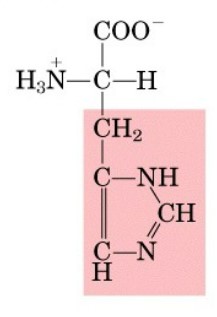
Aminoacidi non polari: Questi aminoacidi hanno catene laterali idrofobiche che non reagiscono con l'acqua. Alcuni esempi sono glicina, alanina, leucina e fenilalanina.
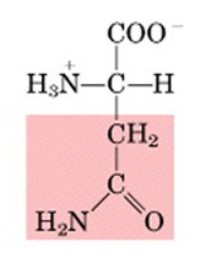
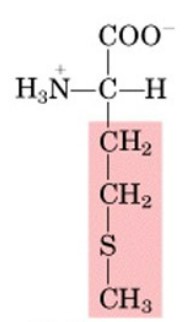
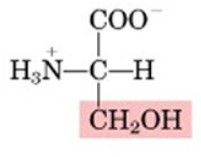
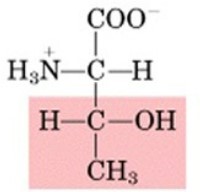
Aminoacidi polari: Questi aminoacidi hanno catene laterali che interagiscono con l'acqua e sono solubili in essa. Esempi sono serina, treonina, cisteina e tirosina.
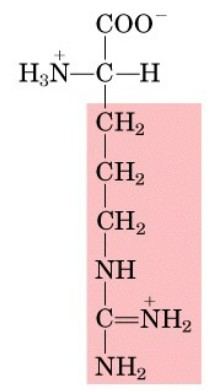
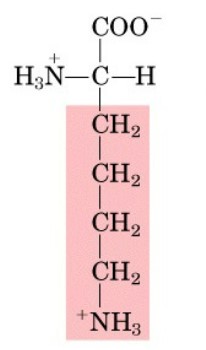
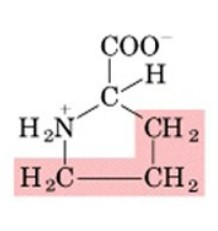
Aminoacidi carichi positivamente (basicità): Questi aminoacidi hanno catene laterali cariche positivamente a pH fisiologico. Esempi sono lisina, arginina e istidina.
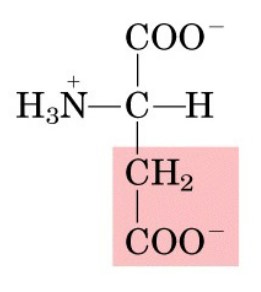
Aminoacidi carichi negativamente (acidità): Questi aminoacidi hanno catene laterali cariche negativamente a pH fisiologico. Esempi sono acido aspartico e acido glutammico.
VISITA Scienzità.it


Nessun commento:
Posta un commento